Российские и китайские ученые совместно разработали нейлоновые нанокапсулы для лечения рака.
Ученые из Института химической биологии и фундаментальной медицины СО РАН вместе с коллегами из онкологической больницы при Медицинском университете Гуанчжоу (Китай) разработали новый метод доставки лекарств к опухолям с использованием нейлоновых нанокапсул. Об этом сообщает издание «Наука в Сибири» СО РАН.
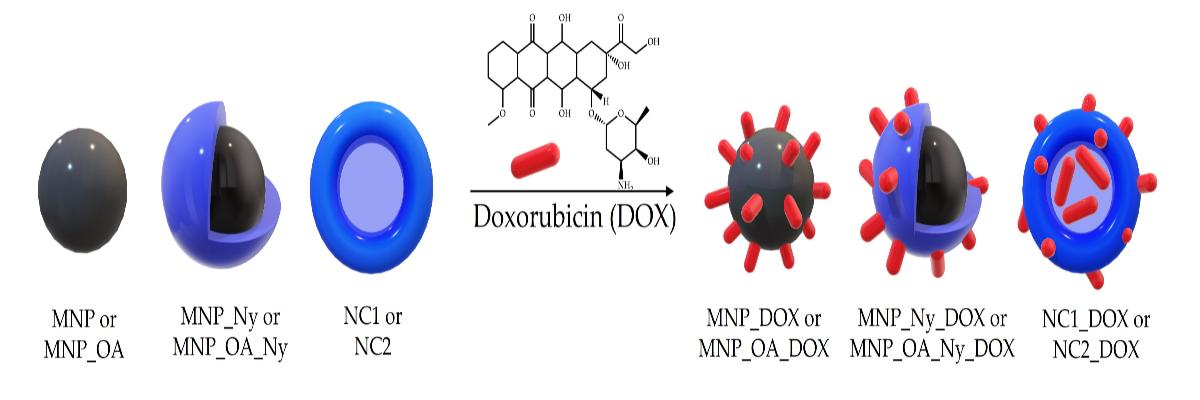
Капсулы состоят из магнитных наночастиц – это позволяет использовать их в МРТ-диагностике и лечении с помощью локальной гипотермии. Некоторые капсулы имеют полую структуру, благодаря чему способны вмещать больше объема лекарств и воздействовать на онкологические новообразования наименее токсичным способом.
Магнитные наночастицы имеют два важных плюса – они управляются внешним магнитным полем, а под воздействием переменного поля разогреваются и вызывают локальный перегрев, из-за которого происходит гибель опухоли.
Несмотря на многие преимущества, наночастицы (смешанный оксид железа Fe3O4) обладают несколькими особенностями: в чистом виде они нестабильны, из-за этого могут вызывать появление активных форм кислорода и повреждать ДНК; в водной среде они способны слипаться – это делает невозможным вводить их внутривенно, а слишком больше частицы забивают капилляры и приводят к тромбозам.
Разработанные препараты являются стабильными: у них не меняются размер, поверхностный потенциал и другие физические характеристики. Они обладают важным качеством – в подобные соединения помещается больше лекарств, а соответственно увеличивается время его удержания в капсуле.
Ученые также надеются, что разработка будет способствовать лечению глиом (опухолей мозга).
Магнитные частицы обладают серьезным недостатком – они способны вызывать мутации, приводящие к возникновению опухолей.
«У нас появилась идея сделать из полимерного покрытия полую капсулу, лишенную магнитного ядра. У такой капсулы нет магнитных свойств, ею нельзя управлять на расстоянии магнитным полем и не получится вызвать с ее помощью локальный разогрев. Но зато в нее можно поместить лекарственный препарат», – говорит Елена Дмитриенко.
Чтобы получить полую капсулу необходима основа (кор), в противном случае полимерная частица сформируется без полости внутри.
Исследователям открываются новые перспективы благодаря возможности химической модификации нейлона с использованием дополнительных агентов. Они способны прикреплять лиганды – молекулы, которые взаимодействуют с рецепторами онкотрансформированных клеток. Это позволяет обеспечить адресную доставку нанокапсул прямо к опухолевым клеткам.
Есть много способов различить раковые клетки от здоровых. Заражённые клетки активно перестраивают свой метаболизм и появляются дополнительные рецепторы на их поверхности. Они уже известны для многих видов рака, и именно на них направлены таргетные препараты.
Можно подобрать лекарство, которое будет специфично подходить к определенному типу раковых клеток, и они сами будут активно поглощать его из кровотока.
Ученые продемонстрировали, что нейлоновые капсулы высвобождают лекарственный препарат в зависимости от pH. Кровоток имеет нейтральный pH, около 7,35-7,45, в то время как онкологические клетки, из-за их активного деления, имеют более низкий pH, то есть они кислее, чем здоровые клетки. Исследователи показали, что чем ниже pH, тем более активно освобождается лекарство из нанокапсул.
В эксперименте в качестве лекарственного препарата использовался доксорубицин, который является одним из основных препаратов для лечения онкологических заболеваний с середины прошлого века. Однако этот препарат является токсичным и плохо усваивается опухолью, поэтому разработка методов его таргетной доставки – важная задача.
Сегодня в мире развиваются методы комплексного воздействия на опухоль с помощью противоракового антибиотика и препаратов на основе терапевтических нуклеиновых кислот.
«Здесь нейлоновые нанокапсулы тоже могут быть полезны. У нас разработаны подходы для присоединения нуклеиновых кислот к нейлону, а в лаборатории биохимии нуклеиновых кислот ИХБФМ СО РАН есть кандидаты в нуклеиновые кислоты, для которых показано, что их проникновение в клетку приводит к подавлению раковой опухоли», — рассказывает Елена Дмитриенко.
Ученые намерены продолжать работу над совершенствованием нанокапсул.
Российские и китайские ученые совместно разработали нейлоновые нанокапсулы для лечения рака.Ученые создали нанокапсулы для лечения рака
Дарья Шевцова
Фото: издание «Наука в Сибири» СО РАН
Ученые из Института химической биологии и фундаментальной медицины СО РАН вместе с коллегами из онкологической больницы при Медицинском университете Гуанчжоу (Китай) разработали новый метод доставки лекарств к опухолям с использованием нейлоновых нанокапсул. Об этом сообщает издание «Наука в Сибири» СО РАН.
Капсулы состоят из магнитных наночастиц – это позволяет использовать их в МРТ-диагностике и лечении с помощью локальной гипотермии. Некоторые капсулы имеют полую структуру, благодаря чему способны вмещать больше объема лекарств и воздействовать на онкологические новообразования наименее токсичным способом.
Магнитные наночастицы имеют два важных плюса – они управляются внешним магнитным полем, а под воздействием переменного поля разогреваются и вызывают локальный перегрев, из-за которого происходит гибель опухоли.
Несмотря на многие преимущества, наночастицы (смешанный оксид железа Fe3O4) обладают несколькими особенностями: в чистом виде они нестабильны, из-за этого могут вызывать появление активных форм кислорода и повреждать ДНК; в водной среде они способны слипаться – это делает невозможным вводить их внутривенно, а слишком больше частицы забивают капилляры и приводят к тромбозам.
Разработанные препараты являются стабильными: у них не меняются размер, поверхностный потенциал и другие физические характеристики. Они обладают важным качеством – в подобные соединения помещается больше лекарств, а соответственно увеличивается время его удержания в капсуле.
Ученые также надеются, что разработка будет способствовать лечению глиом (опухолей мозга).
Магнитные частицы обладают серьезным недостатком – они способны вызывать мутации, приводящие к возникновению опухолей.
«У нас появилась идея сделать из полимерного покрытия полую капсулу, лишенную магнитного ядра. У такой капсулы нет магнитных свойств, ею нельзя управлять на расстоянии магнитным полем и не получится вызвать с ее помощью локальный разогрев. Но зато в нее можно поместить лекарственный препарат», – говорит Елена Дмитриенко.
Чтобы получить полую капсулу необходима основа (кор), в противном случае полимерная частица сформируется без полости внутри.
Исследователям открываются новые перспективы благодаря возможности химической модификации нейлона с использованием дополнительных агентов. Они способны прикреплять лиганды – молекулы, которые взаимодействуют с рецепторами онкотрансформированных клеток. Это позволяет обеспечить адресную доставку нанокапсул прямо к опухолевым клеткам.
Есть много способов различить раковые клетки от здоровых. Заражённые клетки активно перестраивают свой метаболизм и появляются дополнительные рецепторы на их поверхности. Они уже известны для многих видов рака, и именно на них направлены таргетные препараты.
Можно подобрать лекарство, которое будет специфично подходить к определенному типу раковых клеток, и они сами будут активно поглощать его из кровотока.
Ученые продемонстрировали, что нейлоновые капсулы высвобождают лекарственный препарат в зависимости от pH. Кровоток имеет нейтральный pH, около 7,35-7,45, в то время как онкологические клетки, из-за их активного деления, имеют более низкий pH, то есть они кислее, чем здоровые клетки. Исследователи показали, что чем ниже pH, тем более активно освобождается лекарство из нанокапсул.
В эксперименте в качестве лекарственного препарата использовался доксорубицин, который является одним из основных препаратов для лечения онкологических заболеваний с середины прошлого века. Однако этот препарат является токсичным и плохо усваивается опухолью, поэтому разработка методов его таргетной доставки – важная задача.
Сегодня в мире развиваются методы комплексного воздействия на опухоль с помощью противоракового антибиотика и препаратов на основе терапевтических нуклеиновых кислот.
«Здесь нейлоновые нанокапсулы тоже могут быть полезны. У нас разработаны подходы для присоединения нуклеиновых кислот к нейлону, а в лаборатории биохимии нуклеиновых кислот ИХБФМ СО РАН есть кандидаты в нуклеиновые кислоты, для которых показано, что их проникновение в клетку приводит к подавлению раковой опухоли», — рассказывает Елена Дмитриенко.
Ученые намерены продолжать работу над совершенствованием нанокапсул.